科技日報記者 劉霞
人體強大的免疫系統需要精準調控,否則便可能會攻擊我們自身的器官。美國系統生物學研究所的瑪麗·布倫科、索諾瑪生物治療公司的弗瑞德·拉姆斯德爾,以及日本大阪大學的坂口志文,因在“外周免疫耐受”機制方面的突破性發現,共同榮獲2025年諾貝爾生理學或醫學獎。他們的研究揭示了免疫系統如何避免攻擊自身組織,守護人體健康的深層奧秘。
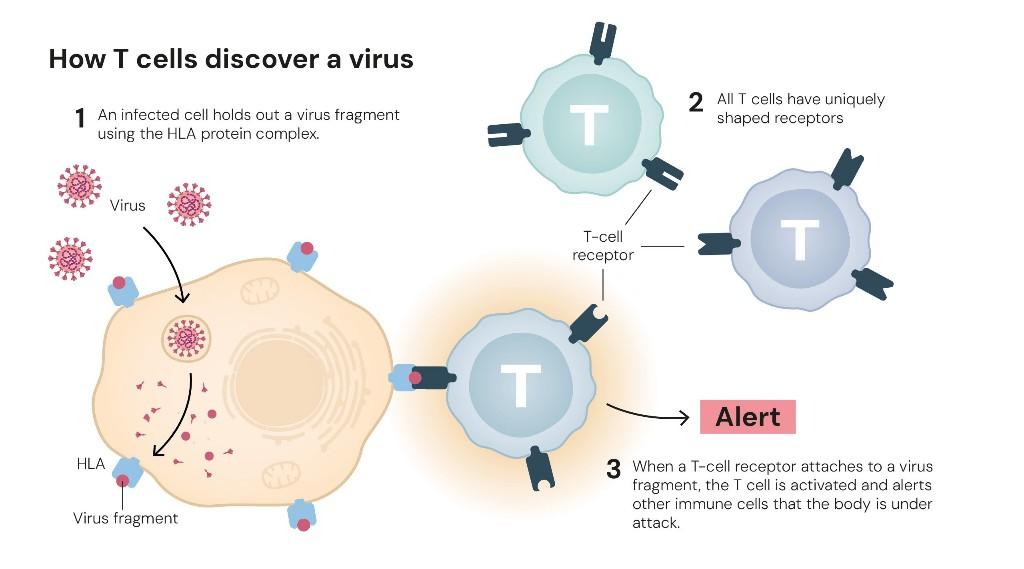
每一天,我們的身體都面臨成千上萬微生物的侵襲,而免疫系統正是抵御這些入侵的忠誠衛士。然而,有些病原體外形多變,甚至能偽裝成人體細胞的“模樣”,以躲避免疫系統的攻擊。那么,免疫系統如何準確分辨敵我,做到既不放過敵人,也不誤傷人體自身組織?
這三位科學家的答案指向了人體內的“調解員”——調節性T細胞。它能夠抑制過度活躍的免疫反應,防止免疫細胞攻擊自身組織。
“他們的發現徹底改變了我們對免疫系統運作機制的理解,解釋了為何大多數人不會患上嚴重的自身免疫疾病。”諾貝爾獎委員會主席歐萊·卡珀如此評價。
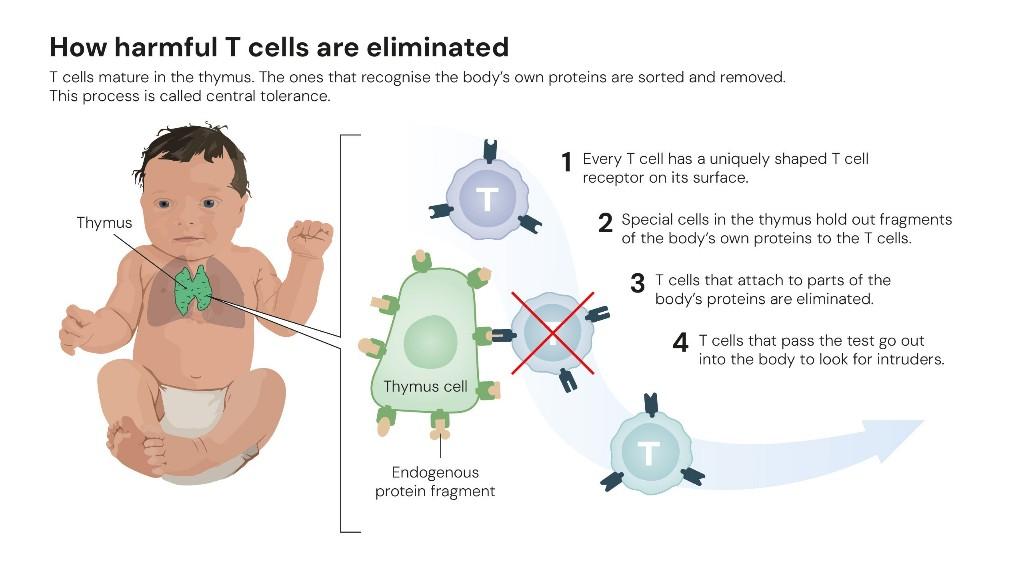
1995年,坂口志文的研究向學界共識發起了挑戰。當時,科學界普遍認為,免疫耐受主要依賴“中樞耐受”過程清除胸腺內可能攻擊自身組織的免疫細胞。然而,坂口志文發現,即便經過中樞耐受過程,仍有一部分具有潛在攻擊性的T細胞會進入外周組織。
他首次識別出一個具有免疫抑制功能的T細胞亞群——調節性T細胞。它們能監測其他免疫細胞,確保免疫系統耐受自身組織,從而防御自身免疫疾病的發生。這一發現為“外周免疫耐受”理論奠定了基礎。
時間來到2001年,布倫科與拉姆斯德爾在研究一種易發多器官自身免疫疾病的小鼠模型時,發現其病因源于關鍵基因FOXP3的突變。進一步的研究顯示,人體內該基因的突變會導致一種罕見而致命的遺傳性自身免疫疾病,即免疫失調、多內分泌腺病、腸病伴X染色體連鎖綜合征。該疾病由FOXP3基因突變引起,造成調節性T細胞功能缺陷,進而引發嚴重的自身免疫反應,累及腸道、內分泌腺和皮膚等多個器官。
兩年后,坂口志文將這兩項重要發現聯系起來,證明FOXP3是調節性T細胞發育與功能的主控基因。缺乏FOXP3的小鼠無法產生功能性調節性T細胞,并迅速出現全身性自身免疫反應。這一關聯性研究不僅確立了調節性T細胞的分子基礎,也標志著該領域進入功能與機制系統解析階段。
如今,調節性T細胞已被公認為免疫穩態的核心調控者。它們如同體內的“巡邏隊”,持續監控其他免疫細胞的活性,確保免疫反應精準而適度,避免誤傷正常組織。

三位獲獎者的研究不僅開創了“外周免疫耐受”這一重要領域,也推動了癌癥與自身免疫疾病的治療進展。基于調節性T細胞的療法正被積極探索,用于治療1型糖尿病、類風濕關節炎等自身免疫病,也有望催生更成功的器官移植手術。
從基礎科學到臨床轉化,布倫科、拉姆斯德爾和坂口志文的研究,逐步精準揭開了人體在防御外敵與維護自我健康之間保持精妙平衡的奧秘,為呵護人類健康,書寫下重要篇章。
(圖片來源:諾貝爾獎官網)